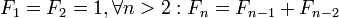در دوران حیات فیبوناچی مسابقات ریاضی در اروپا بسیار مرسوم بود در یکی از همین مسابقات که در سال ۱۲۲۵ در شهر پیزا توسط امپراتورفردریک دوم برگزار شده بود مسئله زیر مطرح شد:
«فرض کنیم خرگوشهایی وجود دارند که هر جفت (یک نر و یک ماده) از آنها که به سن ۱ ماهگی رسیده باشند به ازاء هر ماه که از زندگیشان سپری شود یک جفت خرگوش متولد میکنند که آنها هم از همین قاعده پیروی میکنند حال اگر فرض کنیم این خرگوشها هرگز نمیمیرند و در آغاز یک جفت از این نوع خرگوش در اختیار داشته باشیم که به تازگی متولد شدهاند حساب کنید پس از n ماه چند جفت از این نوع خرگوش خواهیم داشت.»
فرض کنیم xn تعداد جفت خرگوش پس از n ماه باشد، میدانیم که x۲=۱,x۱=۱، تعداد جفت خرگوشها در ماه n+۱ ام برابر خواهد بود با حاصل جمع تعداد جفت خرگوشهایی که در این ماه متولد میشوند با تعداد جفت خرگوشهای موجود(xn).اما چون هر جفت خرگوش که از دو ماه قبل موجود بوده هم اکنون حداقل دوماه سن خواهند داشت و به سن زادو ولد رسیدهاند تعداد جفت خرگوش های متولد شده برابر خواهد بود با xn-۱، پس خواهیم داشت:
x۱ = ۱ , x۲ = ۱ , xn + ۱ = xn + xn - ۱
که اگر از قواعد مذکور پیروی کنیم به دنباله زیر خواهیم رسید که به دنباله فیبوناچی مشهور است.
۱, ۱, ۲, ۳, ۵, ۸, ۱۳, ۲۱, ۳۴, ۵۵, ۸۹, ۱۴۴, ۲۳۳, ۳۷۷, ۶۱۰, ۹۸۷, ۱۵۹۷, ۲۵۸۴,…
فیبوناچی با حل این مسئله از راه حل فوق دنباله حاصل را به جهان ریاضیات معرفی کرد که خواص شگفتانگیز و کاربردهای فراوان آن تا به امروز نه تنها نظر ریاضیدانان بلکه دانشمندان بسیاری از رشتههای دیگر را به خود جلب کرده.
رابطهٔ دنبالهٔ فیبوناچی به این شکل است:
برای مثال برای به دست آوردن جملهٔ دهم باید جملهٔ نهم (۳۴) و جملهٔ هشتم (۲۱) را با هم جمع کنیم که برابر ۵۵ میشود.
جمله عمومی دنباله فیبوناچی[ویرایش]
چند فرمول برای احتساب جملهٔ nام دنبالهٔ فیبوناچی، بدون استفاده از جملات ماقبل وجود دارد.
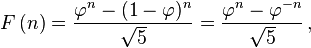 ، یکی از این فرمول هاست.
، یکی از این فرمول هاست.
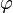 (فی) همان عدد طلایی است که برابر با :
(فی) همان عدد طلایی است که برابر با :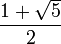 میباشد.
میباشد.
ارتباط عدد طلایی با دنباله فیبوناچی[ویرایش]
روشهای متفاوتی برای بیان رابطه بین عدد طلایی و دنباله فیبوناچی وجود دارد که ما در اینجا به دو نمونه بسنده میکنیم.
نسبت دو عضو متوالی دنباله[ویرایش]
اولین مطلبی که در زمینه ارتباط با دنباله فیبوناچی قابل ذکر است به این قرار است: دنباله را بار دیگر در نظر میبینیم:
۱۰----۹----۸----۷----۶----۵----۴----۳----۲----۱----شماره جمله
۵۵----۳۴----۲۱----۱۳----۸----۵----۳----۲----۱----۱----مقدار جمله
نسبت جمله دوم به اول برابر است با ۱
نسبت جمله سوم به دوم برابر است با ۲
نسبت جمله چهارم به سوم برابر است با ۱٫۵
نسبت جمله پنجم به چهارم برابر است با ۱٫۶۶
نسبت جمله ششم به پنجم برابر است با ۱٫۶
نسبت جمله هفتم به ششم برابر است با ۱٫۶۲۵
نسبت جمله هشتم به هفتم برابر است با ۱٫۶۱۵
نسبت جمله نهم به هشتم برابر است با ۱٫۶۱۹
نسبت جمله دهم به نهم برابر است با ۱٫۶۱۷
به نظر میرسد که این رشته به عدد طلایی نزدیک میشود. اگر نسبت عدد چهلم این رشته را به عدد قبلی حساب کنیم به عدد ۱٫۶۱۸۰۳۳۹۸۸۷۴۹۸۹۵ میرسیم که با تقریب ۱۴ رقم اعشار نسبت طلایی را نشان میدهد. نسبت جملات متوالی به عدد طلایی میل میکند.
معادله خط[ویرایش]
معادلهٔ خطی به صورت y=mx در نظر میگیریم. m به معنی شیب خط است و یک عدد حقیقی است. میدانیم اگر m گنگ باشد، خط y=mx از هیچ نقطهای با مختصات صحیح به جز مبدأ عبور نخواهد کرد. در واقع این خط امکان ندارد از نقطهای (جز مبدأ) عبور کند که هم x و هم y آن عدد صحیح باشند.
حال به جای m قرار میدهیم: φ. یعنی خط y=φx را در نظر میگیریم. چون φ هم یک عدد گنگ است، این خط از هیچ نقطهای با x و y صحیح (جز مبدأ) عبور نخواهد کرد. به همین دلیل نقطههایی را با x و y صحیح در نظر میگیریم که کمترین فاصله را از این خط دارند. ابتدا به نظر میرسد نقطهٔ (۱، ۱) کمترین فاصله را با این خط دارد. ولی فاصلهٔ نقطهٔ (۲، ۱) از این خط کمتر است. نقطهٔ (۳، ۲) فاصلهٔ کمتری با این خط دارد. همچنین فاصلهٔ نقطهٔ (۵، ۳) از این هم کمتر است. این نقاط به همین ترتیب ادامه خواهند یافت و در زیر چند نقطهٔ بعدی را که فاصلهشان از این خط کمتر میشود را میبینید:...،(۵۵، ۳۴)، (۳۴، ۲۱)، (۲۱، ۱۳)، (۱۳، ۸)، (۸، ۵)، (۵، ۳)، (۳، ۲)، (۲، ۱)، (۱، ۱)
صحت مطالب فوق به راحتی قابل بررسی است. با کمی دقت در مختصات این نقاط درخواهیم یافت که این مختصات از الگوی دنباله فیبوناچی پیروی میکنند. این نقاط را نقاط فیبوناچی مینامند.
انواع روش های جداسازی:
هدف از جداسازی ، حذف مزاحمتها ، غلیظ کردن محلول مورد نظر و یا سایر موارد است. برای جداسازی از اختلاف در خصوصیات فیزیکی استفاده میشود، مثل فراریت ، حلالیت و ضریب تقسیم مواد__ و ... . در آنالیز و جداسازی مواد مختلف از تکنیکهای ویژهای برحسب نوع و ساختار مواد و مخلوطها استفاده میشود که برخی از آنها که معروف بوده و حائز اهمیت بیشتری هستند، در زیر میآوریم.
تبلور:
هدف از تبلور ، جداسازی ناخالصی از اجسام جامد است. در این روش ، ابتدا جامد ناخالص را در یک حلال گرم حل میکنند، سپس محلول را صاف میکنند. ناخالصیها در فاز مایع باقی میمانند. اگر تبلور طی چند مرحله صورت گیرد، به آن تبلور جزء به جزء میگویند. در این روش انتخاب حلال از اهمیت بالایی رخوردار است. اگر از تکنیک ذوب برای جداسازی ناخالصی از جامد استفاده شود، به آن تصفیه ذوب گویند.این روش در جدا کردن ناخالصیهای ژرمانیم و اسید بتروییک کاربرد دارد. در این فرآیند ، ضریب تقسیم برابر با نسبت غلظت ناخالصی در فاز جامد به غلظت ناخالصی در فاز مایع است.
|
فرایند تبلور
|
| علوم طبیعت > شیمی > شیمی فیزیک > شیمی بلور | -->(cached) |

| تبلور یک ماده ، عبارتست از جهت یافتگی ذرهای و آرایش مولکولی و تثبیت این نظم در فضای ماده. |
تاریخچه بلورشناسی
فلاسفه قدیم نیز منشاء بلورهای یک سنگ را بلورهای یخ میدانستند که بر اثر تحمل سرمای بسیار شدید در طول مدت مدید ، طوری سخت و مقاوم شده است که میتواند حرارتهای بالاتر از صفر را هم تحمل نماید. در سال 1690 ، "Huyghens" دریافت که بلورها از اجتماع ذرات کوچکتر بوجود آمدهاند و در سال 1912 ، "M.V.Laue" توانست تئوری ساختمان شبکهای در بلورها را با استفاده از اشعه ایکس به اثبات برساند.
تبلور و نمو بلورها
تبلور معمولا در موقع تبدیل یک حالت فیزیکی به حالت فیزیکی دیگر صورت میگیرد. این تبدیل به سه صورت زیر انجام میشود:
تبلور در هنگام تبدیل حالت مایع به جامد
- انجماد مواد مذاب :
اگر ماده مذاب به سرعت سرد شود، اتمها یا مولکولها با هر موقعیتی که دارند، متراکم و بیحرکت میشوند و ماده منجمد میگردد. در این صورت جسمی جامد و ایزوتوپ بدون داشتن نظم ذرهای تشکیل میشود. اگر سرد شدن با آرامی و کند انجام شود، اتمها و مولکولها با توجه به نیروی جاذبه خود و اطاعت از شبکه تبلور کنار هم چیده شده و نطفه بلور را تشکیل میدهند. سپس در نتیجه اتصال سایر مولکولهای منزوی و معلق در ماده مذاب به نطفه بلور ، حجم آن افزایش مییابد تا اینکه به بلوری درشت تبدیل میگردد. - تبلور مواد محلول :
در این نوع تبلور باید محلول به حال فوق اشباع باشد. در چنین محلولهایی بلورها تشکیل و تهنشین میشوند. این بلورها ابتدا به صورت نطفههای متحرک میباشند، علت تحرک آنها حرکات قبلی یونها و مولکولهای سازنده آنها است. در محلولها نیز مانند انجماد مواد مذاب ، رشد بلورها از طریق اتصال منظم یونها ، اتمها و مولکولهای معلق در محلول به نطفههای بلور صورت میگیرد.
تبلور در هنگام تبدیل حالت بخار به جامدسوبلیماسیو ن
در این حالت تبلور ، بلورها مستقیما از تبدیل بخار به جامد حاصل میشوند. این بلورها معمولا کوچک و دارای طرح اولیه میباشند که اصطلاحا اسکلت بلور گفته میشود. در طبیعت ، سوبلیماسیون در گازهای خشک آتشفشانی دیده میشود. در این حالت مواد گازی آتشفشانی در شکافهای توده آذرین مستقیما به بلور تبدیل میگردند. مثال بسیار روشن برای پدیده سوبلیمانسیون ، تشکیل قشرهای بلور یخ ناشی از انجماد مستقیم بخار آب اطاقها بر روی شیشه پنجرهها در سرمای زمستان میباشد.
تبلور مواد جامد
حالت سوم تبلور که خوب شناخته نشده و در طبیعت فراوان دیده میشود، تبلور در محیط جامد است. در این حالت رشد بلورها بخرج بلورهای کوچکتر و تحت تاثیر فشار و حرارت و در مدت زمان طولانی صورت میگیرد. برای مثال امروزه سنگهای شیشهای آتشفشانی خیلی قدیمی را متبلور میبینیم. بنابراین معلوم میشود که این گونه سنگها به تدریج در طول زمان متبلور شدهاند. سنگهای آهکی دانه ریز که از بلورهای ریز کربنات کلسیم تشکیل شدهاند، تحت تاثیر عوامل دگرگونی (فشار و حرارت) به مرمر که دارای بلورهای دانه درشت کلسیت است، تبدیل میگردد.
تاثیر عوامل خارجی در نمو بلورها
شرایط زیر سبب بوجود آمدن اختلاف در اندازه بلورها میگردد:
-
سرعت انجماد :
افزایش طول مدت انجماد یک ماده مذاب امکان تغذیه شیمیایی بیشتر بلورها از ماده مذاب را فراهم میسازد. بنابراین کم شدن سرعت انجماد ، موجب تشکیل بلورهای درشت و تسریع در انجماد سبب تشکیل بلورهای کوچک و ریز میگردد. ۱-وجود مواد فرار :
وجود بخار آب و گازها در یک ماده مذاب ، نقطه انجماد را پایین آورده و سرعت انجماد را کند میسازد. بنابراین باعث افزایش رشد بلورهای آن ماده میشود. به عنوان مثال در رگههای پگماتیت به علت وجود بخار آب و گازهای فراوان در ماده مذاب پگماتیتی ، بلورها به مراتب درشتتر از بلورهای توده آذرین اصلی است، حال آنکه سرعت انجماد در رگههای پگماتیت از سرعت انجماد توده آذرین اصلی بیشتر بوده است.
۲-تراکم محلول :
اندازه بلورها در یک محلول بستگی به درجه اشباع شدگی آن محلول دارد. در محلولهای فوق اشباع تعداد مراکز تبلور فراوان میباشد و در نتیجه اندازه بلورها کوچک خواهد شد. برعکس در محلولهائی با درجه اشباع شدگی کمتر تعداد مراکز تبلور کم بوده و بنابراین اندازه بلورها درشتتر خواهد بود.
میانبار یا ادخال در بلورها
در حین رشد بلور ممکن است موادی به صورت جامد ، مایع و یا گاز به سطح بلور بچسبد. ادامه رشد بلور باعث میشود که این مواد در درون بلور قرار گرفته، موجب تشکیل ادخال در داخل بلور گردد، حبابهایی خیلی کوچک گاز کربنیک همراه با آب در داخل بلور کوارتز و یا قطرات خیلی کوچک آب در بلورهای نمک طعام و نیز قطرات مواد مذاب غیر متبلور (شیشه) در درون بلورهای فلدسپات ادخالهائی میباشند که همزمان با تبلور بلور در داخل آن قرار میگیرند.
اجتماع بلورها
اجتماع بلورها به دو صورت اجتماع منظم و نامنظم مشاهده میشود:
-
اجتماع نامنظم :
در این نوع ، اجتماع بلورها در جهات مختلف بدون رعایت نظم و ترتیب صورت میگیرد. مثلا در یک توده نبات یا در اختلاط گچ زنده با آب میبینیم که گچ میبندد. سخت و یکپارچه شدن این ماده به علت تبلور مجدد بلورهای ژیپس و چسبیدن آنها به یکدیگر صورت میگیرد. -
اجتماع منظم :
هرگاه در زمان تشکیل و نمو بلورها ، شرایط مناسب باشد، نطفههای بلور بطور اتفاقی در کنار هم نمیگیرند، بلکه طبق قواعد معین با نظم و ترتیب خاصی با یکدیگر ، رشد و نمو خواهند نمود. صورتهای مختلف اجتماع منظم بلورها عبارتند از:-
اجتماع کروی (اسفرولیتی) :
اگر تبلور ماده مذاب سریع صورت بگیرد و تعداد مراکز تبلور کم باشد، بلورها به شکل سوزنهای باریک و به صورت دستجات کروی و جدا از هم تشکیل میشوند، مانند بلورهای سوزنی شکل طلا و کلرور پتاسیم که در سیستم کوپیک متبلور میشوند. -
اجتماع موازی :
در این گونه تجمع ، بلورها بطور موازی در کنار یکدیگر قرار میگیرند و دارای سطوح مشترکی میباشند. در اجتماع موازی بلورها معمولا بلورهای همجنس شرکت دارند، مانند بلور کوارتز. -
اجتماع بلورهای غیرهمجنس :
علاوه بر بلور همجنس ، بلورهای غیرهمجنس نیز به نوبه خود تشکیل اجتماع منظم و یا جهتدار میدهند. این نوع اجتماعات بر پایه تشکیل نطفه بلوری بر روی بلور دیگری قرار دارد، به نحوی که سطح مشترک بین دو بلور از نظر ساختمان شبکهای مشابه باشند. برای مثال ، اغلب بر روی بلورهای ورقهای هماتیت بلورهای سوزنی شکل روتیل نمو نمودهاند و در پگماتیتها بلورهای کوارتز در داخل بلور ارتوز به صورت اجتماع موازی دیده میشود.
-

اختصاصات مواد متبلور
اجسام متبلور به خاطر داشتن شکل مخصوص ، سختی ، خاصیت ارتجاعی ، مقاومت محدود در مقابل حرارت و فشار و نقطه ذوب از مایعات و گازها متمایز میشوند. بعضی از مواد متبلور مانند پارافین نرم هستند و اجسامی مانند شیشه و پلاستیک هرچند که جامدند، ولی متبلور نمیباشند. بلورها اجسامی همگن و انایزوتوپ هستند. انایزوتوپ بودن بلور به این علت است که اختصاصات فیزیکی مانند سرعت انتشار حرارت و نور یا درجه سختی و غیره در جهات موازی آنها برابر میباشد و در جهات مختلف نابرابر میباشد.
رنگ بلورها
هرگاه بخش اعظم نور از بلور عبور کند و فقط مقدار کمی از آن جذب گردد، بلور شفاف دیده میشود و چنانچه مقدار نور جذب شده و نوری که از بلور عبور میکند، تقریبا برابر باشد، بلور نیمه شفاف به نظر میرسد. در صورتی که اگر تمام نور وارده جذب گردد، بلور تیره دیده میشود. هرگاه جذب نور برای طول موجهای مختلف متفاوت باشد، بلور رنگی بنظر میرسد.
بعضی از بلورها دارای رنگهای مشخص هستند، مثلا مالاکیت دارای رنگ سبز و ازوریت دارای رنگ آبی آسمانی میباشد. تعدادی از بلورها در اصل بیرنگ میباشند، ولی در اثر وجود ناخالصی و یا پیگمان به رنگهای مختلفی دیده میشوند. مثلا کوارتز بیرنگ بوده، ولی در اثر ناخالص دارای رنگهای سفید ، بنفش ، دودی ، زرد ، صورتی و سیاه میباشد و یا وجود کروم به صورت پیگمان در کروندوم باعث رنگ قرمز آن میشود.
برخی از کاربردهای بلورها
-
بلورهای
 و نظایر آنها در ساختن وسایل نوری بکار میروند.
و نظایر آنها در ساختن وسایل نوری بکار میروند. -
بلورهائی با خاصیت پیروالکتریسته مثل
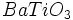 در صنعت الکترونیک کاربرد دارند.
در صنعت الکترونیک کاربرد دارند. -
بلورهای SiC در تهیه ترانزیستور و روبین یا یاقوت در تهیه اشعه لیزر مورد استفاده قرار میگیرند.
بلورها برحسب نوع ذرات تشکیل دهنده و نیروهای نگه دارنده این ذرات به چهار نوع بلورهای یونی ، مولکولی ، کووالانسی (مشبک) ، فلزی گروه بندی میشوند
تقطیر:
اگر هدف از تقطیر ، جداسازی یک مخلوط به اجزای بالا باشد، از تقطیر ساده برای جداسازی اجزاء استفاده میشود. اما اگر همه اجزاء فرار باشند، از تقطیر جزء به جزء برای جداسازی استفاده میشود. اگر یک مخلوط تولید آزئوتروپ کند، ( مثل آب و الکل) نمیتوان از روش تقطیر جزء به جزء ، اجزای آن را جدا کرد. برای جداسازی این مخلوط از روشهای تقطیر با بخار آب ، تقطیر در خلاء و تقطیر ناگهانی استفاده میکنند.
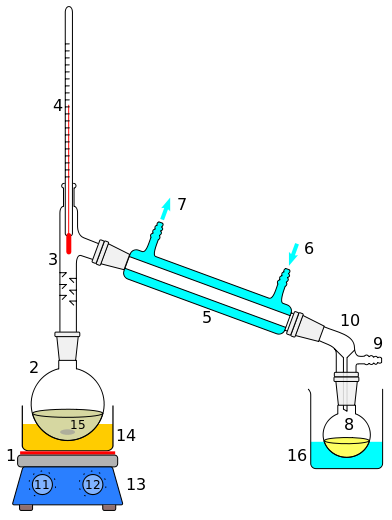
در تقطیر با بخار آب هیچگاه درجه حرارت تقطیر از نقطه جوش آب بیشتر نمیشود. ترکیباتی نظیر تولوئن ، اتیلن ، گلیسیرین و اسیدهایچرب از این طریق جدا میشوند. برای جلوگیری از تجزیه مایعاتی که دارای نقطه جوش بالایی هستند از تقطیر در خلاء استفاده میشود. با کاهش فشار ، نقطه جوش مایع کاهش پیدا میکند.در تهیه آب آشامیدنی از آب دریا و تهیه آب مقطر نیروگاهها از تقطیر ناگهانی استفاده میشود. در این روش مایع بطور مداوم وارد و بخار بطور مداوم خارج میشود. در شکل زیر تصویر
یک دستگاه تقطیر دیده می شود.
تصویری از یک نمومه آزمایشگاهی دستگاه تقطیر: 1: گرمکن 2: بالن تقطیر 3: برج تقطیر 4: دماسنج(برای تعیین دمای جوش) 5: مبرد 6: ورودی آب سرد 7: خروجی آب سرد 8: بالن جمع آوری محصول 9: ورودی گاز یا خلاء 10: جمع آوری کننده بخارات 11: تنظیم کننده حرارت 12: تنظیم کننده سرعت همزن 13: صفحه گرمکن 14: حمام روغن یا شن 15: همزن 16: حمام آب سرد.
رسوب دادن:
نوعی روش جداسازی است که اساس آن اختلاف حلالیت اجسام میباشد. یعنی جزیی که حلالیت کمتری دارد زودتر جدا میشود. با افزایش نیروی جاذبه سرعت تهنشین شدن افزایش پیدا میکند. عمل سانتریفوژ در واقع بر همین اساس است.
سانتریفیوژ (به انگلیسی: Centrifuge) یا دستگاه مرکزگریز دستگاهی است که در آن با استفاده از نیروی گریز از مرکز مواد را از یکدیگر جدا میکنند. در این دستگاه محفظهای که مواد جداشدنی در آن قراردارد معمولاً به کمک یک موتور به سرعت حول یک محور میچرخد.
سانتریفوژ دستگاهی است که از آن برای چرخاندن مواد با سرعت بالا استفاده میشود. دانشمندان معمولاً دستگاه سانتریفوژ را برای جدا کردن ذرات جامد از یک مایع یا تقسیم مخلوط مایعات به اجزای مختلف آن به کار میگیرند. مخلوط را درون لولهای قرار میدهند که طوری قرار داده شدهاست که با چرخش دستگاه، به سمت خارج از مرکز حرکت میکند و به حالت افقی قرار میگیرند. در این حالت، نیروی گریز از مرکز میخواهد که مخلوط را برخلاف مرکز سانتریفوژ براندو از این نقطه دور کند و ذرات یا مایع سنگین تر بیش تر به سمت بیرون (یا ته مخلوط) رانده میشوند. وقتی سانتریفوژ از حرکت باز میایستد، مواد به همین حالت غیر مخلوط میمانند. خون و سایر نمونههای بیولوژیکی را معمولاً به وسیله دستگاه سانتریفوژ جدا میکنند. سریعترین سانتریفوژ با نام «فرامرکز گریز» با سرعت ۲۰۰۰۰۰ دور در دقیقه میچرخد. از دستگاههای گریز از مرکز بزرگ برای انجام آزمایش بر روی خلبانان نظامی و فضانوردان استفاده میشود تا میزان مقاومت آنان در شتابهای بالا معلوم شود.
انواع دستگاه ها
انواع دستگاههای مرکز گریز برای مصارف گوناگون ساخته شدهاست. نمونههای خانگی این دستگاه برای جداکردن آب از سبزیها مثل کاهو و غیره بکار میرود. همچنین در ماشینهای لباسشویی نیز برای خشک کردن لباس استفاده میشود. در نمونههای آزمایشگاهی برای جداکردن گلوبولهایخون از پلاسما استفاده میشود. دستگاههای صنعتی با موتورهای قوی و در ابعاد بزرگ برای جدا کردن مواد بکار میرود. در کار غنیسازی اورانیوم نیز از دستگاههای مرکزگریز گازی استفاده میشود.
اساس کار سانتریفوژها
هر گاه جسمی با سرعت معینی حول یک مرکز با محور دوران کند نیرویی در جسم متحرک و در جهت عمود بر مسیر دوران و به سمت خارج از مرکز ایجاد میگردد. که به نیروی فراگریز یا نیروی گریز از مرکز موسوم است که مقدار آن از رابطه F=MRW2 که در آن R شعاع دوران M جرم جسم و V سرعت خطی و W سرعت زاویهای است بدست میآید. محور دوران ممکن است به سه حال قائم، افقی یا مایل باشد.

استخراج:
اساس این روش ، اختلاف حلالیت یک جزء در دو حلال غیر قابل حل در یکدیگر است. اگر دو حلال غیر قابل استخراج ، مایع باشند، به این روش استخراج مایع ـ مایع گویند و اگر یک جسم جامد به وسیله یک حلال استخراج شود، به آن استخراج جامد ـ مایع گویند (مثل استخراج اسانسها ، عصارهها و روغن از دانههای گیاهی). عموما دو فاز مورد استفاده ، یکی آب است و دیگری یک حلال آلی.مقداری از جسم در فاز آبی و مقداری نیز در فاز آلی میباشد. بازده استخراج با ضریب تقسیم نسبت مستقیم دارد. دوبار استخراج با حجم کمتر از حلال آلی همیشه موثر از یک بار استخراج با حجمی مساوی دو برابر حجم اول است. چون در حالت اول ، مقدار وزن ماده باقیمانده محلول در آب ، کمتر از حالت دوم خواهد بود.
کروماتوگرافی:
اساس کروماتوگرافی ، جذب سطحی مواد و توزیع آنها در دو فاز میباشد. یکی از فازها ثابت و فاز دیگر متحرک است که نمونه مورد نظر در فاز متحرک جدا میشود. فاز ثابت یا جامد است و یا مایع و فاز متحرک یا مایع است و یا گاز . اگر فاز ثابت ، جامد و فاز متحرک ، مایع باشد، به آن کروماتوگرافی مایع ـ جامد LSC ) )گویند. اگر فاز متحرک ، گاز و فاز ثابت ، جامد باشد، به آن کروماتوگرافی گاز - جامد ( GSC ) گویند. اگر فاز متحرک ، مایع و فاز ثابت نیز مایع باشد به آن کروماتوگرافی مایع ـ مایع LLC ) یا( HPLC گویند و در نهایت اگر فاز متحرک ، گاز و فاز ثابت ، مایع باشد، به آن کروماتوگرافی گاز - مایع GLC ) یا (VPC گویند.در LSC ، جدا شدن بر اساس جذب سطحی یا تعریض یونها و یا تشکیل کمپلکس میباشد. در GSC اساس ، جداسازیجذب سطحی است. در LLC و GLC ، مواد بر اساس توزیع بین دو فاز جدا میشوند. پس کروماتوگرافی روشی برای جداسازی مخلوط بدلیل اختلاف تحرک آنها میباشد.کروماتوگرافی LSC در واقع نوعی کروماتوموگرافی جذبی است که مواد بر اساس اختلاف در قابلیت جذب خود روی سطح جامد از یکدیگر جدا میشوند. در GSC نیز اساس جداسازی جذب سطحی فاز گاز روی سطح جامد است. از این روش برای خالص سازی گازها استفاده میشود.
کروماتوگرافی لایه نازک(Thin Layer Chromatography) (TLC)
کروماتوگرافی لایه نازک نوعی کروماتوگرافی جذبی جامد – مایع است و اصول آن مانند کروماتوگرافی ستونی است. ولی در این مورد جسم جاذب جامد را به صورت یک لایه نازک در روی یک قطعه شیشه یا پلاستیک محکم پخش میکنند. یک قطره از محلول نمونه یا مجهول را در نزدیکی لبه صفحه میگذارند و صفحه را همراه مقدار کافی از حلال استخراج کننده در ظرفی قرار میدهند. مقدار حلال باید آنقدر باشد که فقط به سطح زیر لکه برسد (شکل الف). حلال به طرف بالای صفحه میرود و اجزاء مخلوط را با سرعتهای متفاوت با خود میبرد. در نتیجه ممکن است تعدادی لکه روی صفحه ظاهر شود. این لکه ها روی یک خط عمود بر سطح حلال ظرف قرار میگیرند (شکل ب).

این روش کروماتوگرافی بسیار آسان است و به سرعت هم انجام میشود. این روش برای تفکیک اجزاء یک مخلوط بسیار مفید است و همچنین میتوان از آن برای تعیین بهترین حلال استخراج کننده جهت کروماتوگرافی ستونی استفاده کرد.
در TLC میتوان از همان مواد جامد که در کروماتوگرافی ستونی استفاده میشود استفاده کرد و در این میان سیلیکا و آلومینا بیشتر به کار میرود. معمولا جسم جاذب را با مقدار کمی از ماده نگهدارنده مانند گچ شکسته بندی، کلسیم سولفات و یا نشاسته مخلوط میکنند تا جسم جاذب چسبندگی لازم را پیدا کند و به صفحه بچسبد. صفحه ها را میتوان قبل از مصرف تهیه کرد و یا از ورقه های پلاستیکی آماده که در بازار موجود است استفاده نمود.
یکی از مزایای مشخص TLC آن است که احتیاج به مقدار بسیار کمی از نمونه دارد. در بعضی موار میتوان تا مقدار 9-10 گرم را تشخیص داد. اما ممکن است اندازه نمونه تا 500 میکرو گرم برسد. در نمونه های زیاد میتوان از تجربه های تهیه ای استفاده کرد. در این تجربه ها لکه های مختلف را میتراشند و با یک حلال مناسب میشویند (استخراج میکنند). و برای شناسایی (از طریق طیف سنجی) به کار میبرند.
تشخیص لکه های رنگین در روی کروماتوگرام آسان است و برای تعیین محل لکه های اجسام بیرنگ روشهای متعددی وجود دارد. برای مثال میتوان با تابش نور ماوراء بنفش به صفحه محل لکه، ترکیبهایی را که خاصیت فلوئورسانس دارند مشخص کرد. به روش دیگر میتوان جسم جاذب را با ماده فلوئورسانس دار بی اثر دیگری مخلوط کرد. هنگامی که نور ماوراء بنفش به این صفحه بتابد، لکه اجسامی که نور ماورای بنفش را جذب ميکنند ولی خاصیت فلوئورسانس ندارند در زمینه فلورسانس دار صفحه به صورت تیره رنگ ظاهر میشوند. در بسیاری موارد دیگر، از معرفهای آشکارساز دیگری استفاده میکنند. این معرفها را میتوان بر روی کروماتوگرام پاشید و لکه ها را ظاهر کرد. سولفوریک اسید، که بسیاری از ترکیبات آلی را به ذغال تبدیل میکند و محلول پتاسیم پرمنگنات نمونه هایی از معرفهای آشکار ساز هستند که به این روش مصرف میشوند. ید نیز معرف آشکار ساز دیگری است که مصرف میشود. در این مورد صفحه را در ظرفی میگذارند که محیط آن از بخار ید اشباع باشد. بسیاری از ترکیبات آلی ید را جذب میکنند و لکه آنها روی کروماتوگرام رنگین (معمولا قهوه ای) میشود.
در شرایط معین سرعت حرکت ترکیب نسبت به سرعت پیشرفت حلال (Rf) خاصیت مشخصی از ترکیب است. برای تعیین این مقدار مسافتی را که جسم از خط شروع تا وسط لکه را طی کرده است اندازه میگیرند و آنرا به مسافتی که حلال پیموده تقسیم میکنند. این مسافت را با خط شروع یکسانی میسنجند.
بخش عملی
تفکیک مواد رنگی برگ سبز
چند میلی لیتر از مخلوط 2 به یک اتر نفت و اتانول را همراه با چند برگ سبز در هاونی بگذارید و برگها را با دسته هاون له کنید. مایع بدست آمده را به یک قیف جدا کننده منتقل کنید و همان حجم آب مقطر به آن اضافه کنید و تکان دهید. فاز آبی پایینی را دور بریزید. این شستشو را دو بار انجام دهید و هر بار فاز آبی را دور بریزید. و آب تازه اضافه کنید.لایه آلی (بالایی) را به ارلن کوچکی منتقل کنید و به آن 2 گرم سدیم سولفات بدون آب اضافه کنید (برای آب گیری).
یک نوار 10 سانتی از ورقه کروماتوگرام سیلیکاژل تهیه کنید و یک لکه 1 الی 2 میلی متری از محلول ماده رنگی را طوری بر روی صفحه قرار دهید که حدود 1 و نیم سانتی متر از انتهای آن فاصله داشته باشد (برای گذاشتن لکه از لوله مویین تمیز استفاده کنید). صبر کنید تا لکه خشک شود. برای جداسازی، از حلال بنزن – استون با نسبت 7 – 3 (حجمی) مطابق توضیحات بالا استفاده کنید.
ممکن است تا هشت لکه رنگین مشاهده شود. این لکه ها به ترتیب کاهش مقدار Rf عبارتند از کاروتنها (دو لکه نارنجی)، کلروفیل a (آبی – سبز)، کلروفیل b (سبز) و زانتوفیلها (چهار لکه زرد).
یکی از کلیشهایترین و شاید تاریخیترین سوالهای دانشآموزان درخصوص درس ریاضی این است که ریاضی و فرمولهای متعدد آن در زندگی ما چه کاربردی دارد.
برای پاسخگویی به این سوال با همکاری دانش آموزان دبیرستان نمونه دولتی حیدری موسوی شهرستان هشترود، کارگاهی آموزشی درباره عدد 1.618 و کاربردهای آن برگزار کردیم. گذشته از نحوه گروه بندی، اجرا و جزئیات این طرح ـ که برای نخستین بار در آموزش و پرورش کشور انجام شد ـ در این طرح که طرحی نو در آموزش ریاضی است، موضوعات مختلف و کاربردی- ریاضی درسیکه در سطح بین الملل نیز دارای تازگی و پویایی است ـ مورد بررسی قرار گرفت.
نسبت طلایی یا همان عدد 1.618 یکی از زیبایی های دنیای ریاضی است که در گوشه و کنار این دنیای بزرگ از اندام های بدن انسان تا آثار برجسته و مشهور هنری و معماری در سطح دنیا و حتی نحوه رشد دانه های گل آفتابگردان می توان ردپایی از آن پیدا کرد. بسیاری از کارشناسان بر این باورند هر اثر هنری که در آن نسبت طلایی رعایت شده باشد، منحصر به فرد است. جالباین که در کاغذهای استاندارد سری A نیز نسبت طول به عرض با نسبت طلایی برابر است. به همین دلیل، محققان بر این باورند زیباترین سطوح و اشکال آنهایی است که نسبت طلایی در آنها به کار رفته باشد.
عدد 1.618 که به عدد یا نسبت طلایی یا نسبت فیبوناچی نیز شهرت دارد، حاصل تلاش دانشمندانی ازجمله اقلیدس، لوکاپاچیولی و لئوناردو فیبوناچی است. شما می توانید در حوزه های مختلف ردپایی از نسبت طلایی را پیدا کنید. یکی از این حوزه ها هندسه است. اگر در پاره خطی، نسبت قسمت بزرگ تر به کوچک تر برابر با نسبت کل خط به قسمت بزرگ باشد، این نسبت قطعا عدد طلایی است.
یکی دیگر از حوزه هایی که نشانی از نسبت طلایی در آن پیدا می کنید، دنباله فیبوناچی است. در این دنباله که عبارت است از 1، 1، 2، 3، 5، 8، 13، 21 و... اگر اعداد پس از 2 را در نظر بگیریم و هر کدام را به عدد ماقبل خود تقسیم کنیم، شاهد اعدادی بسیار نزدیک به عدد نسبت طلایی یا 1.618 خواهیم بود. هر چه بیشتر این تقسیم را ادامه دهید، عدد حاصل به نسبت طلایی نزدیک تر می شود.
گذشته از این در بسیاری از ساختارهای هستی می توانید نشانی از نسبت طلایی پیدا کنید؛ از مارپیچ های دی ان ای گرفته تا مارپیچ گوش انسان، حلزون، ساختار مارپیچی کهکشان ها و تمام زیبایی های طبیعت ازجمله برگ های درختان، خطوط و نقش و نگار روی پرهای طاووس و مارپیچ های آفتابگردان این نسبت رعایت شده است. این عدد در معماری باستان و معاصر ایران و جهان نیز کاربرد فراوانی داشته است. از آن جمله می توان به هرم جیزا در مصر، برج آزادی تهران، قلعه دالاهو در کرمانشاه، بنای بیستون کرمانشاه و مقبره ابن سینا در همدان اشاره کرد. برای مثال ابعاد بنای بیستون کرمانشاه پنج کیلومتر در سه کیلومتر ذکر شده که اعداد چهارم و پنجم دنباله فیبوناچی اند. با تقسیم این دو عدد به عدد 1.6 می رسیم که بسیار نزدیک به عدد طلایی است.
این عدد در بدن انسان نیز بسیار کاربرد دارد. زیبایی چهره، زیبایی خنده، تناسب اندام و خوش تیپی همه و همه از شاهکارهای الهی در آفرینش انسان است. اگر نگاهی به تاریخچه عدد طلایی بیندازید، می بینید لئوناردو داوینچی اولین نفری است که نسبت دقیق استخوان های انسان را اندازه گیری و ثابت کرد این نسبت ضریبی از عدد طلایی است. در سنجش تناسب اندام خود می توانید فاصله انگشتان پا تا ناف را بر فاصله ناف تا بالای سر تقسیم و حاصل را با عدد 1.618 مقایسه کنید. هر چه این عدد به 1.618 نزدیک تر باشد به این معنی است که شما تناسب اندام خوبی دارید. چنین نشانه هایی که در آنها می توان به نسبت طلایی رسید، در بدن انسان بسیار زیاد است. یکی از دیگر ویژگی های جالب توجه نسبت طلایی این است که اگر فاصله شهر مکه تا قطب شمال را بر فاصله این شهر تا قطب جنوب تقسیم کنیم، عددی بسیار نزدیک به عدد طلایی به دست می آید. بر این اساس می توان گفت شهر مکه در نقطه طلایی زمین قرار دارد. علاوه بر این، بررسی های انجام شده نشان داده است شهر مکه در نقطه طلایی عربستان و بنای کعبه در نقطه طلایی شهر مکه قرار دارد.